
NOS PREGUNTAN

Principal reglamentación en materia de salud en el 2025
- Fabiola Alba Muñoz
- Febrero 4 de 2026
- 1:00 PM
En esta edición, como es habitual, hemos compilado la principal reglamentación expedida para el sector salud durante el 2025, clasificada por temáticas con el fin de facilitar su lectura.
En el contexto general de la actividad legislativa, las discusiones en el órgano legislativo se dieron en torno a las reformas promovidas por el Gobierno nacional. En junio del 2025, terminando la tercera legislatura, se aprobó la Ley 2466 que introdujo cambios importantes en la jornada laboral, los recargos nocturnos, cambios al contrato de aprendizaje, entre otros. La reforma al sistema de salud por el contrario surtió aprobación en el segundo debate y al terminar la legislatura, en el tercer debate, fue archivado en la comisión séptima de Senado. Esta decisión fue apelada por el Gobierno y al cierre de esta edición aún no se conocía la disposición final sobre el proyecto
También se sancionó la Ley 2475 o derecho al olvido oncológico, una propuesta que busca asegurar la inclusión y no discriminación de las personas sobrevivientes de cáncer. También la Ley 2006, que fomenta la investigación científica y tecnológica para combatir microorganismos multirresistentes y prevenir la resistencia antimicrobiana.
Desde el Ejecutivo se emitió normatividad relacionada con el Modelo de Salud Preventivo, Predictivo y Resolutivo en Salud que fuera suspendido posteriormente por el Consejo de Estado, la puesta en marcha del Sistema Integral de Información Financiera y Asistencial (SIIFA), la operación de los equipos básicos de salud, la autorización para negociar conjuntamente entre entidades promotoras de salud (EPS) la adquisición de tecnologías en salud, la reiteración de inembargabilidad de los recursos de salud y sus excepciones, la reglamentación de la operación de las mesas de trabajo con actores del sistema para analizar la suficiencia de la UPC en cumplimiento a la orden novena del Auto 007 de la Corte Constitucional, la Política Pública del Talento Humano en Salud y la emergencia sanitaria por fiebre amarilla.
También se expidió el Plan Nacional de Salud Rural (PNSR), actualizaciones de los servicios y tecnologías con y sin cargo a la UPC, actualización de la Clasificación Única de Procedimientos en Salud (CUPS), modificaciones a la línea de crédito con tasa compensada Findeter, la ampliación de plazo para la implementación CIE 11, la clasificación de riesgo de las Empresas Sociales del Estado (ESE), entre otras temáticas.
En materia de inspección, vigilancia y control, se prorrogaron las medidas de intervención forzosa para administrar de la mayoría de EPS intervenidas. La medida de intervención de la EPS Sanitas fue revocada. Por parte del ente de vigilancia y control también se ordenó la modificación de condiciones de algunos reportes de información de sus vigilados.
A manera ilustrativa relacionamos, según las temáticas más importantes, la normatividad expedida:
A. Flujo de recursos
- Resolución 2316 (12 de noviembre). Anexo técnico de viabilidad de los proyectos de la línea “Desarrollo Sostenible de las Regiones-Sector Salud de Findeter. La presente resolución tiene por objeto sustituir el anexo técnico de la Resolución 1146 del 2023, en virtud de la cual se estableció el procedimiento, los requisitos de viabilidad de los proyectos de la línea de redescuento con tasa compensada de la Financiera de Desarrollo Territorial S. A. (Findeter) “Desarrollo Sostenible de las Regiones-Sector Salud”, con el propósito de incluir a las Instituciones Prestadoras de Servicios de Salud (IPS) de carácter mixto y a los hospitales universitarios que se encuentren en proceso de acreditación, para el financiamiento de la infraestructura para el Desarrollo Sostenible de las Regiones-Sector Salud.
- Resolución 2067 (6 de octubre). Reintegro de los recursos del Sistema General de Seguridad Social en Salud (SGSSS), apropiados o reconocidos sin justa causa. Con la presente resolución se modifican los artículos 5 y 6 la Resolución 1716 del 2019 mediante la cual establece el procedimiento de reintegro de los recursos del SGSSS, apropiados o reconocidos sin justa causa, con el propósito de disminuir los tiempos relativos al término de respuesta a la solicitud de aclaración en quince días y a la elaboración de informe por la entidad encargada del reintegro a diez días, en pro de garantizar los principios de economía, eficacia y debido proceso de la actuación administrativa.
- Circular 32 (29 de septiembre). Inembargabilidad de los recursos del SGSSS. A través de la presente circular el Ministerio de Salud y Protección Social reitera el alcance del principio de inembargabilidad de los recursos públicos destinados a la salud, destacando su fundamento constitucional, legal, su naturaleza parafiscal y de destinación específica. Por tanto, los recursos del SGSSS solo pueden ser afectados de manera excepcional y bajo condiciones estrictas. El precedente constitucional vigente ha delimitado las condiciones para exceptuar el principio general de inembargabilidad de los recursos de la salud correspondientes al Sistema General de Participaciones (SGP) en los siguientes términos: (1) que se trate de obligaciones de índole laboral; (2) que estén reconocidas mediante sentencia, y (3) que se constate que para satisfacer dichas acreencias son insuficientes las medidas cautelares impuestas sobre los recursos de libre destinación de la entidad territorial deudora.
Así mismo, con respecto a las rentas del Presupuesto General de la Nación, admite excepciones orientadas a garantizar la seguridad jurídica y el respeto de derechos reconocidos en sentencias judiciales. De este modo, los procedimientos y plazos aplicables al pago de créditos judiciales deben ser los mismos que para otras obligaciones estatales, incluidas las provenientes de actos administrativos o contratos, especialmente los créditos laborales reconocidos judicialmente, siempre que se compruebe la insuficiencia de otros recursos disponibles, entre otras excepciones.
En dicho marco se instruye a los prestadores y actores del sistema a hacer uso preferente de los mecanismos de conciliación y las instancias de coordinación para la prevención de conflictos, a garantizar la continuidad en la prestación de los servicios de salud a todos los usuarios y a abstenerse de promover medidas cautelares sobre recursos que, por su naturaleza, son inembargables, así como de invocar medidas de embargo como justificación para suspender o negar dichos servicios.
- Resolución 2025160000004979-6 (20 de junio). Mesa de Trabajo suficiencia de la Unidad de Pago por Capitación (UPC) en cumplimiento de la orden novena del Auto 007 de la Corte Constitucional. Mediante la presente resolución, la Superintendencia Nacional de Salud crea la Mesa de Trabajo para para analizar las denuncias relacionadas con la información que se reporta para el cálculo de la UPC, las actuaciones desplegadas en ella, y los resultados obtenidos conforme lo dispuesto en la orden novena del Auto 007 del 2025 proferido por la Sala Especial de Seguimiento de la Corte Constitucional con ocasión de la valoración de las órdenes vigésima primera y vigésima segunda de la Sentencia T-760 del 2008, relativa a la suficiencia de la UPC.
- Resolución 1122 (30 de mayo). Categorización del riesgo de las Empresas Sociales del Estado (ESE) del nivel territorial para la vigencia 2025. Mediante la presente resolución se realiza la categorización del riesgo de las ESE del nivel territorial para la vigencia 2025, una vez aplicada la metodología prevista en la Resolución 2509 del 2012, modificada por la Resolución 2249 del 2018. Por lo anterior, los saldos de los recursos del Fondo de Salvamento y Garantías para el Sector Salud (Fonsaet) con que cuentan las entidades territoriales, no distribuidos o no ejecutados por estas, se destinarán al financiamiento de los Programas de Saneamiento Fiscal y Financiero viabilizados o que se viabilicen por el Ministerio de Hacienda y Crédito Público.
- Decreto 572 (28 de mayo). Tarifas para retención en la fuente. El Ministerio de Hacienda y Crédito Público eleva la tarifa de autorretención en la fuente para las actividades económicas señaladas en el decreto, con el objetivo de aumentar el recaudo durante el año gravable 2025, por lo cual se pagará de manera anticipada una parte del impuesto de renta correspondiente al 2026. Así mismo, los porcentajes de retención por otros ingresos tributarios será máximo del 4,5 % del respectivo pago o abono en cuenta. El presente decreto entró en vigor a partir del 1.º de junio del 2025 y las antiguas medidas serán se aplicaron hasta el 31 de mayo del 2025.
Resolución 757 (30 de abril). Modifica el listado de procedimientos de laboratorio clínico financiados con recursos de la UPC. Modifica el “Anexo 3. Listado de procedimientos de laboratorio clínico financiados con recursos de la UPC” de la Resolución 2718 del 2024, en el sentido de incluir el código CUPS 90.8.8.56 “Identificación de otro virus (específica) por pruebas moleculares” exclusivamente para SARS CoV2 como se muestra en la figura 1.

- Resolución 630 (9 de abril). Tarifas de unidades de valor tributario (UVT) Cannabis. Fija las tarifas en unidades de valor básico (UVB), para el pago de los servicios de evaluación y seguimiento, así como los criterios para las devoluciones a que haya lugar por la prestación de los servicios a los titulares de las licencias de semillas para siembra y grano, cultivo de plantas de cannabis psicoactivo, cultivo de plantas de cannabis no psicoactivo y licencias extraordinarias para el cultivo de plantas de cannabis, así como para el pago de los servicios de seguimiento de las licencias de fabricación de derivados de cannabis, de fabricación de derivados no psicoactivos de cannabis y extraordinaria de fabricación de derivados por investigación no comercial derivadas de la Ley 1787 del 2016. Lo anterior no aplica para las tarifas y los demás aspectos relacionados con los servicios de evaluación de las licencias de fabricación de derivados de cannabis, de fabricación de derivados no psicoactivos de cannabis y extraordinaria de fabricación de derivados por investigación no comercial derivadas de la Ley 1787 del 2016.
- Resolución 370 (28 de febrero). Mesa de trabajo trabajo para análisis de la UPC. Crea la mesa de trabajo de carácter participativo en cumplimiento del Auto 007 del 2025 y se establecen las reglas para su funcionamiento, en armonía con lo establecido en el considerando 22 del Auto 089 del 2025 de la Corte Constitucional. La mesa de trabajo tendrá como objeto recibir, analizar y socializar información, insumos y aportes de los participantes sobre un eventual rezago en el valor de la UPC de las vigencias 2021, 2022, 2023 y 2024, con el fin de que el Ministerio de Salud y Protección Social cuente con elementos de juicio suficientes para determinar técnicamente si hay lugar o no a efectuar el reajuste de la prima.
Resolución 67 (21 de enero). Disposiciones unificadas y contenido metodológico marco que rige el presupuesto máximo. Mediante la presente resolución se ajustan las disposiciones que rigen el presupuesto máximo asignado a las EPS y Entidades Adaptadas (EA) para el patrocinio de los servicios y tecnologías en salud no financiadas con recursos de la UPC y no excluidas de la financiación con recursos públicos asignados a la salud en los componentes de procedimientos de salud, medicamentos, alimentos para propósitos médicos especiales (APME) y servicios complementarios, con el fin de establecer las disposiciones unificadas y el contenido metodológico marco bajo el cual debe desarrollarse el presupuesto máximo y, en general, las directrices que deben observarse para la asignación y el seguimiento de los recursos, en cumplimiento de lo ordenado por Sala Especial de Seguimiento a la Sentencia T-760 del 2008, mediante Auto 2881 del 2023, dentro del seguimiento a las ordenes vigésimo primera y vigésimo segunda en relación con la suficiencia del presupuesto máximo para cubrir la prestación de servicios de salud no cubiertos con recursos de la UPC.
B. Cobertura y atención a los usuarios
- Resolución 2100 (14 de octubre). Política integral para la prevención, la reducción de riesgos y daños y la atención del consumo de sustancias. La presente resolución tiene por objeto adoptar la “Política integral para la prevención, la reducción de riesgos y daños y la atención del consumo de sustancias psicoactivas, lícitas e ilícitas 2025-2033” y el Sistema Nacional de Atención al consumo de sustancias psicoactivas, contenidas en el anexo técnico, el cual será objeto de publicación en la página web del Ministerio de Salud y Protección Social. La política tiene como propósito orientar y garantizar una respuesta integral al consumo de sustancias psicoactivas, basada en la evidencia científica libre de conflicto de interés y respetuosa de los derechos humanos para la población habitante del territorio colombiano, con un especial énfasis en las poblaciones expuestas a condiciones que generan vulnerabilidad, que inciden de manera diferencial en el consumo de sustancias psicoactivas y sus consecuencias.
- Resolución 2068 (6 de octubre). Política Pública para la Prevención, Diagnóstico Temprano y Tratamiento Integral de la Endometriosis 2025-2035. Tiene por objeto (1) adoptar la Política Pública para la Prevención, Diagnóstico Temprano y Tratamiento Integral de la Endometriosis, la cual será objeto de publicación en la página web del Ministerio de Salud y Protección Social; (2) definir las condiciones para la operatividad del Registro de Pacientes con Endometriosis, y (3) establecer las intervenciones para la garantía de los derechos de las personas con endometriosis en el entorno laboral en cumplimiento de lo ordenado en la Ley 2338 del 2023, de conformidad con la parte considerativa del presente acto administrativo.
- Resolución 1968 (24 de septiembre). Programa de Atención Psicosocial y Salud Integral a Víctimas. Adopta medidas para la dirección y la operación del Programa de Atención Psicosocial y Salud Integral a Víctimas, en relación con el desarrollo de las estrategias de atención integral en salud, coordinación intersectorial, asistencia técnica, formación al talento humano e investigación, así como los procesos transversales de participación activa de las víctimas, monitoreo y seguimiento y planeación y gestión financiera, los cuales conducirán a su ejecución y a la articulación y la complementariedad técnica, operativa y territorial de los servicios para la atención integral en salud con enfoque psicosocial, de conformidad con la parte considerativa del presente acto administrativo.
- Circular 029 (27 de agosto). Vacunación Fiebre Amarilla en Gestantes. Imparte directrices para la vacunación de la población gestante contra la fiebre amarilla (FA), a partir de la semana doce de gestación, residente en zonas de muy alta circulación del virus y transmisión activa del brote, previa valoración riesgo. De este modo, las IPS deberán implementar las acciones señaladas en la circular, de las cuales destacamos las siguientes: realizar la búsqueda y ofrecer la vacunación contra la fiebre amarilla a la población gestante que no ha sido vacunada contra la FA, a partir de las doce semanas de gestación, residente o que no le sea posible evitar la permanencia o desplazamiento a veredas con circulación activa del virus de FA, es decir las veredas con evidencia de casos humanos o epizootias en los últimos seis meses, incluyendo las establecidas en el corredor ecoepidemiológico y diligenciar de forma obligatoria el consentimiento informado. Para la vacunación se requiere valoración médica individualizada de riesgo/beneficio, entre otras medidas.
- Resolución 1786 (4 de septiembre). Ruta de atención exposición asbesto. Adopta el lineamiento técnico y operativo de la Ruta Integral para la Atención en Salud para las personas, familias y comunidades con potencial exposición al asbesto o con enfermedades relacionadas al asbesto, el cual será objeto de publicación en la página web del Ministerio de Salud y Protección Social. Sin perjuicio de la obligatoriedad de brindar las atenciones e intervenciones definidas en los lineamientos técnicos y operativos de la ruta que refiere este acto administrativo, las entidades y los prestadores de salud a quienes aplica esta resolución, en el marco de sus competencias, adaptarán la atención en salud acorde a las circunstancias del territorio y considerando el enfoque territorial y diferencial.
- Resolución 1789 (4 de septiembre). Regiones y subregiones funcionales para la gestión. Determina las regiones y subregiones funcionales para la Gestión Territorial Integral de la Salud Pública y, así mismo, establece la metodología para su tipificación, organización y actualización en el marco del proceso de territorialización del Modelo de Salud Preventivo, Predictivo y Resolutivo, que se encuentra detallada en los anexos técnicos que serán objeto de publicación en la página web del Ministerio de Salud y Protección Social, de conformidad con la parte considerativa del presente acto. Cada uno de los actores involucrados en el ámbito de la aplicación de la presente resolución lo harán en el marco de sus respectivas competencias asignadas por la normativa vigente. Se contará con un periodo de seis meses, contados a partir de la publicación de esta norma, para adecuarse a lo previsto en este acto administrativo.
- Decreto 858 (30 de julio). Modelo de Salud Preventivo, Predictivo y Resolutivo (suspendido provisionalmente). Mediante el presente decreto se sustituye la parte 11, del Libro 2 del Decreto 780 del 2016, con el fin de adoptar el Modelo de Salud Preventivo, Predictivo y Resolutivo como política en salud para la población habitante en el territorio colombiano. El modelo se fundamenta en la Atención Primaria en Salud (APS) y busca el cuidado integral de la salud de las personas, las familias y las comunidades en los territorios, mediante la acción coordinada de los actores del sector salud, los otros sectores y la comunidad en general, desarrollando atributos de accesibilidad, primer contacto longitudinalidad, integralidad, coordinación, interdisciplinariedad, transectorialidad y participación social. Su despliegue se realiza a partir de una construcción colectiva de base territorial que integra como principios la interculturalidad, la igualdad, la no discriminación y la dignidad, buscando la superación de inequidades en el abordaje de determinantes sociales de la salud y la transformación social.
El Modelo de Salud Preventivo, Predictivo y Resolutivo establece como pilares o líneas estratégicas los siguientes: (1) gobernabilidad, gobernanza y territorialización; (2) Redes Integrales e Integradas Territoriales de Salud (RIITS); (3) trabajo digno y decente para el talento humano en salud y otros trabajadores del sector; (4) soberanía sanitaria y gestión del conocimiento, y (5) Calidad y Sistema Integrado de Información de la Atención Primaria en Salud (SI-APS).
- Circular 026 (9 de julio). Prohibición de afectación en la continuidad de los servicios de salud en La Guajira. Prohíbe que cualquier autoridad político-administrativa interrumpa la prestación del servicio de salud que actualmente se materializa en el departamento de La Guajira, especialmente a través de los hospitales de campaña o móviles, so pena de que se inicien por parte de los organismos correspondientes las acciones penales, disciplinarias y fiscales a que haya lugar. La Superintendencia Nacional de Salud deberá, en el marco de sus funciones de inspección, vigilancia y control garantizar que las autoridades administrativas correspondientes no impidan u obstaculicen la prestación de los servicios de salud en los hospitales móviles o de campaña referenciados y, de ser el caso, impondrá las sanciones correspondientes.
- Ley 2475 (9 de julio). Establece y garantiza el derecho al olvido oncológico en Colombia y se dictan otras disposiciones. Tiene por objeto establecer y garantizar el derecho al olvido oncológico, con la finalidad de asegurar la inclusión y la no discriminación de las personas sobrevivientes de cáncer, bajo los siguientes principios: (1) confidencialidad de la historia clínica: se reafirma el carácter reservado de la historia clínica de los pacientes, en consonancia con el derecho a la intimidad y la protección de datos personales. La divulgación de cualquier información relativa al diagnóstico o tratamiento oncológico queda supeditada al consentimiento expreso del paciente, salvo en los casos taxativamente señalados por la ley; (2) reconocimiento de la doble victimización: se reconoce la doble victimización que enfrentan las personas sobrevivientes de cáncer, manifestada tanto en la duración del tratamiento como una vez superada la enfermedad, lo que implica las secuelas psicológicas, sociales y laborales derivadas de su condición; (3) principio de no discriminación: se prohíbe cualquier forma de discriminación basada en antecedentes oncológicos, especialmente en el acceso a servicios financieros, laborales, educativos y de salud, y (4) principio de inclusión social: se promoverán políticas públicas y acciones afirmativas que garanticen la igualdad de oportunidades y la participación de las personas sobrevivientes de cáncer en la sociedad.
- Resolución 1182 (9 de junio). Proceso de asignación de afiliados de la población no indígena e indígena que no hacen parte del territorio CRIC afiliada a la Asociación Indígena del Cauca. Tiene por objeto, en el marco de la ruta de transición hacia el sistema indígena de salud propio e intercultural, de que trata el artículo 54 del Decreto Ley 968 del 2024: “Por el cual se dictan normas para la administración y operatividad del Sistema Indígena de Salud Propio e Intercultural (SISPI) para el Territorio Indígena que conforma el Consejo Regional Indígena del Cauca (CRIC)”, activar el proceso de asignación de afiliados de la población no indígena e indígena que no hacen parte del territorio CRIC que está afiliada a la Asociación Indígena del Cauca, Entidad Promotora de Salud Indígena (AIC-EPS-I), identificada con NIT 817.001.773-3, a la(s) EPS o EPS-I receptora(s).
- Resolución 401 (10 de marzo). Estrategia de acompañamiento psicosocial para población migrante, ponderación para la asignación de recursos. Adopta la estrategia de acompañamiento psicosocial para población migrante, población colombiana retornada y comunidades de acogida o receptoras, la cual se encuentra en el anexo técnico que hace parte integral de esta resolución; también determina los criterios habilitantes y de ponderación para la asignación de los recursos para su implementación.
La presente resolución está dirigida a las ESE y las entidades territoriales que resulten priorizadas en razón de su territorio para la implementación de la estrategia de acompañamiento psicosocial para población migrante, población colombiana retornada y comunidades de acogida o receptoras. Los recursos serán dirigidos a la implementación de la estrategia de manera sucesiva y gradual de conformidad con la disponibilidad de recursos con los que se cuente en los municipios que se requiera, los cuales deberán ser viabilizados por la Oficina de Promoción Social del Ministerio de Salud.
- Circular 09 (10 de marzo). Reglas unificadas para la atención de pacientes con complicaciones por biopolímeros e implantes mamarios. De esta manera, en cumplimiento de la Sentencia SU-239 del 2024, relacionada con las reglas unificadas para la atención en salud de pacientes con complicaciones causadas por sustancias modelantes invasivas e inyectables no permitidas —biopolímeros e implantes mamarios—, el Ministerio de Salud y Protección Social establece que ante complicaciones derivadas de procedimientos cosméticos o estéticos, cuando sea necesario garantizar el derecho a la vida e integridad de las personas conforme el criterio del médico tratante, debe garantizarse la atención de salud por parte de las EPS a sus afiliados.
Así, los procedimientos de retiro de biopolímeros e implantes mamarios se establecen en la CUPS Resolución 2641 del 2024, modificada por la Resolución 2689 del 2024, como se muestra en la tabla 2.
Tabla 2. Código CUPS para retiro de biopolímeros e implantes mamarios

- Resolución 309 (20 de febrero). Autonomía progresiva y contextual de niños, niñas y adolescentes a través del asentimiento y el proceso de consentimiento informado. Imparte lineamientos para garantizar la participación en la toma de decisiones en salud y el ejercicio de la autonomía progresiva y contextual de niños, niñas y adolescentes, mediante el asentimiento pediátrico y el proceso de consentimiento informado en las atenciones en salud de acuerdo con el concepto de autonomía progresiva y contextual, desde el enfoque de derechos humanos, género, diferencial étnico, curso de vida, discapacidad, territorial, y bajo la comprensión del marco de los derechos individuales y colectivos que están contenidos en esta resolución y su anexo técnico, el cual hace parte integral del presente acto administrativo.
- Circular 04 (6 de febrero). Prevalencia del derecho fundamental a la salud de los niños, niñas y adolescentes-vacunación fiebre amarilla. Con la presente circular se recuerda que la vacunación es indispensable en la contención de la enfermedad viral fiebre amarilla (FA), coadyuvando a la protección de la persona y evitando consigo consecuencias letales o secuelas graves. Por lo anterior, todos los niños, niñas y adolescentes tienen el derecho a que la vacuna contra la FA les sea suministrada, por lo cual los padres de familia deben apoyar la decisión que se adopte por los menores frente a esta, así dicha decisión se encuentre en contra de sus creencias, cultura o religión. Lo anterior tiene sustento en una ponderación de derechos fundamentales, donde prevalecen los derechos fundamentales a la vida y a la salud. El Ministerio de Salud y Protección Social denunciará ante el Instituto Colombiano de Bienestar Familiar (ICBF), y demás autoridades competentes, los casos en los cuales los padres de menores de edad se interpongan en el suministro de vacuna, puesto que ello menoscaba los derechos fundamentales de estos.
C. Medicamentos, insumos y dispositivos médicos
- Resolución 1811 (4 de septiembre). Uso de equipos generadores de radiación ionizante, prestación de servicios de protección radiológica y control de calidad. La presente resolución tiene por objeto reglamentar tanto el uso de equipos generadores de radiación ionizante y su control de calidad en prácticas médicas, veterinarias, industriales o de investigación, el otorgamiento de las licencias para el ejercicio de dichas prácticas, así como la prestación de servicios de protección radiológica. El Ministerio de Salud y Protección Social dispondrá en su página web los formatos que desarrollan el contenido de la presente resolución.
- Circular 027 (29 de julio). Gestión de importación y compra de medicamentos vitales no disponibles. Teniendo en cuenta que las EPS están obligadas a reformular el tratamiento con un medicamento equivalente y asegurar su entrega efectiva, y establecer canales de comunicación claros y eficientes con los usuarios para informar sobre el punto de dispensación, la fecha de entrega y la persona responsable del suministro, para proteger el derecho fundamental a la salud y evitar la interrupción de tratamientos médicos esenciales, mediante la presente circular se conmina a las EPS para que hagan uso de los mecanismos normativos y procedimientos especiales descritos en el Decreto 481 del 2004 con la finalidad de evitar el desabastecimiento de aquellos medicamentos VITALES no disponibles y, en consecuencia, importe y adquiera los medicamentos necesarios para suplir las necesidades en materia de salud de sus afiliados.
- Resolución 914 (15 de mayo). Manual de Requisitos para la Implementación de las Buenas Prácticas de Reprocesamiento de Dispositivos Médicos y Elementos Reutilizables (DMER). Adopta el Manual de Requisitos para la Implementación de las Buenas Prácticas de Reprocesamiento de Dispositivos Médicos y Elementos Reutilizables (DMER) que han sido definidos como reutilizables por el fabricante. Se excluyen los procesos de repotenciamiento, remanufactura y otros procedimientos cuya intención sea restaurar las condiciones y especificaciones de seguridad y rendimiento establecidas por el fabricante del dispositivo original, o cuyo propósito sea modificar el uso, así como los dispositivos médicos de un uso (DMUU).
- Resolución 35379 (10 de junio). Autorización para negociar conjuntamente entre EPS la adquisición de tecnologías en salud. De este modo la Superintendencia de Industria y Comercio autorizó la solicitud de aplicación del parágrafo único del artículo 1 de la Ley 155 de 1959, de las EPS Sanitas, Asmet Salud, Emssanar, Famisanar, Nueva EPS, Savia Salud, EPS-SOS, Capresoca y Coosalud, esto es, la celebración de un acuerdo para negociar de manera conjunta la adquisición de tecnologías en salud para que, una vez realizada la negociación, cada una de las intervinientes en el acuerdo puedan adquirir y distribuir estas tecnologías. Dicho acuerdo estará dividido en tres etapas, en las cuales se planea negociar diferentes tipos de medicamentos, dispositivos médicos y alimentos con propósitos médicos.
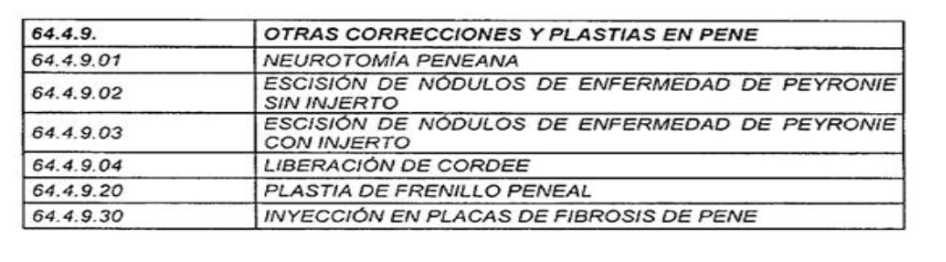
- Resolución 756 (30 de abril). Modifica CUPS. Con la presente resolución se modifica la categoría “64.4.9. OTRAS CORRECCIONES Y PLASTIAS EN PENE” del Anexo Técnico 2 “Lista tabula” de la Resolución 2641 del 2024, modificada a su vez por la Resolución 2689 del 2024, en el sentido de incluir la subcategoría “64.4.9.20 PLASTIA DE FRENILLO PENEAL”, como se muestra en la tabla 3.
Tabla 3. Resolución 756 del 2025
- Circular 17 (9 de mayo). Implementación de la ruta operativa para la distribución, suministro y seguimiento del medicamento antirretroviral para VIH. Imparte las directrices para la implementación de la ruta operativa en la cual se incluyen los procedimientos para la distribución, el suministro y el seguimiento a la dispensación del medicamento a los usuarios por parte de las EPS y Entidades Adaptadas o quien haga sus veces, IPS o gestores farmacéuticos, asegurando que llegue de manera oportuna a los siguientes grupos de personas con diagnóstico de VIH mencionados en el artículo 1 de la Resolución 2164 del 2024: personas que viven con VIH que hacen parte de la población migrante venezolana regular, personas que viven con VIH recién diagnosticadas y personas que viven con VIH con falla virológica.
- Resolución 542 (31 de marzo). Compra centralizada, distribución y suministro de los medicamentos para el tratamiento de enfermedades huérfanas. Establece los criterios bajo los cuales el Ministerio de Salud y Protección Social, a través del Fondo Rotatorio Regional para la Adquisición de Productos Estratégicos de Salud Pública OPS/OMS, podrá realizar la compra centralizada de medicamentos cuyas indicaciones sean específicas y únicas para el tratamiento de enfermedades huérfanas contempladas en la Resolución 023 del 2023 o la norma que la modifique o sustituya, señalando pautas para su distribución y suministro, así como las reglas para el seguimiento de los medicamentos entregados.
- Resolución 0525 (28 de marzo). Modifica Guía para el desarrollo y presentación de los estudios de estabilidad de medicamentos de síntesis química. Modifica el anexo técnico de la Resolución 3157 del 2018 para optimizar la respuesta regulatoria y operativa frente a los cambios estratégicos de la industria farmacéutica y a su vez impactar positivamente en la recuperación de capacidad de manufactura de dicha industria, que permita atender oportunamente la demanda de medicamentos en el mercado. Así mismo, establece qué documentos de naturaleza eminentemente técnica, como lo es el anexo técnico de la resolución en mención, puedan tener un proceso de actualización más expedito lo cual es más factible si estos se expiden como guías por parte del Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) en los términos del artículo 6 del Decreto 334 del 2022 o aquel que lo modifique o sustituya.
D. Procedimientos, instrucciones y reportes de información
- Resolución 2065 (6 de octubre). Autorización de sedes transitorias o itinerantes para prestar servicios de salud en situaciones excepcionales o de emergencia. Tiene por objeto definir las condiciones mínimas de operación de los servicios de salud en sedes transitorias o itinerantes con infraestructura adaptada o unidades móviles terrestres o fluviales, en situaciones excepcionales o de emergencia que afecten o limiten el acceso efectivo a los servicios de salud, de conformidad con la parte considerativa del presente acto. Los servicios de salud que se presten en las sedes transitorias deberán cumplir los requisitos mínimos establecidos en el manual que adopta la Resolución 3100 del 2019 para situaciones de emergencia y los descritos en el anexo técnico que hace parte integral de la presente resolución. Se podrá autorizar la operación de sedes transitorias para prestar servicios de salud por un término de hasta doce meses, prorrogables hasta por una vez sin exceder los veinticuatro meses, previa justificación, mientras persistan las condiciones que dieron lugar a la situación excepcional o de emergencia.
- Resolución 2053 (2 de octubre). Modifica estatuto de contratación ESE-proyectos de infraestructura y de dotación biomédica. Mediante la presente resolución se modifica el artículo 9 de la Resolución 5185 del 2013, modificado por el artículo 1 de la Resolución 1440 del 14 de agosto del 2024, respecto a la regla de aplicación existente para la contratación de obras de adecuación, ampliación y construcción de infraestructura y de dotación biomédica cuya fuente de financiación sean recursos del Presupuesto General de la Nación, en el sentido de que, cuando el Ministerio de Salud y Protección Social considere viable, la ESE pueda hacer uso de su manual, previa autorización de esta cartera ministerial.
- Circular 101 (22 de septiembre). Lineamientos jornadas de trabajo Reforma Laboral. El Ministerio de Trabajo brinda una herramienta que facilita la interpretación y aplicación de lo dispuesto en la Reforma Laboral (Ley 2466 del 2025), estableciendo los lineamientos generales para garantizar el cumplimiento de las disposiciones normativas en materia de jornada de trabajo, jornada aplicable a los servicios domésticos, jornada máxima en casos de remuneración a destajo, registro y control de horas extras, límites al trabajo suplementario y reglas sobre la remuneración en días de descanso obligatorio. Esta circular se configura como un mecanismo institucional para atender las disposiciones generales en relación con la promoción de condiciones laborales dignas, prevenir prácticas contrarias a la ley y orientar a empleadores y trabajadores en la adecuada aplicación de la normatividad vigente.
- Resolución 1963 (23 de septiembre). Comité Institucional de Salud Rural del Plan Nacional de Salud Rural. Conforma el Comité Institucional de Salud Rural como un órgano de coordinación, implementación, seguimiento y evaluación de las acciones estratégicas contenidas en el Plan Nacional de Salud Rural (PNSR), de conformidad con la parte considerativa del presente acto administrativo. El Comité Institucional de Salud Rural deberá aprobar y dar seguimiento al Plan de Acción del Plan Nacional de Salud Rural, formular acciones preventivas y correctivas derivadas de dicho seguimiento y gestionar su implementación y financiamiento, conforme a sus competencias.
- Circular 31 (15 de septiembre). Uso emblemas personal sanitario, Lineamiento Equipos Básicos de Salud. Partiendo de los lineamientos vigentes de la Estrategia de Fortalecimiento de la Gestión Territorial en Atención Primaria en Salud (APS), en cuya relación con los Equipos Básicos de Salud (EBS) y su operación a nivel territorial ha implicado el despliegue de un importante volumen de personal sanitario en los departamentos, se identifica una necesidad imperiosa de unificar los mecanismos de identificación, emblematización y visibilización de los integrantes de los EBS. Esta situación se ha abordado conforme a lo previsto en la Resolución 4481 del 2012, que establece medidas para la protección y el respeto del ejercicio de la Misión Médica en Colombia. Por tanto, mediante la presente circular se imparten instrucciones para el uso de emblemas por parte del personal sanitario, lineamiento técnico de la estrategia de Fortalecimiento de la Gestión Territorial en Atención Primaria de Salud (APS), con respecto a los Equipos Básicos de Salud (EBS) y su operación a nivel territorial, el cual hace parte integral del presente acto.
- Resolución 1905 (17 de septiembre). Modifica procedimiento CUPS. Con la presente resolución se modifica la Resolución 3804 del 2016, con el propósito de establecer que la Clasificación Única de Procedimientos en Salud (CUPS) se actualizará con una prioridad de dos años, o por un menor tiempo cuando las condiciones del sistema así lo requieran. Así mismo, se refuerzan los requerimientos técnicos de la nominación para que las demás fases del procedimiento puedan surtirse de manera satisfactoria, al tiempo de no considerar necesario el levantamiento de actas de cada sesión realizada. La entrada en vigencia de la presente resolución se establece a partir del 1.º de enero del 2026.
- Resolución 1962 (23 de septiembre). Estructura del Sistema Integral de Información Financiera y Asistencial (SIIFA). Tiene por objeto desarrollar la estructura SIIFA, la información a registrar y su oportunidad en cada uno de sus módulos; las responsabilidades de los agentes del sector salud obligados al registro de información; los manuales de usuario, funcionales, técnicos de interoperabilidad, y demás disposiciones necesarias para su funcionamiento, de conformidad con la parte considerativa del presente acto administrativo.
En dicho contexto, los prestadores de servicios de salud, proveedores de tecnologías en salud y los fabricantes, importadores y titulares de registro sanitario cuando realicen ventas masivas a las EPS y otros pagadores, con excepción de las entidades con objeto social diferente, deberán verificar y registrar en el SIIFA la aceptación de la información de los acuerdos de voluntades suscritos, previamente registrados por las entidades responsables de pago. Los prestadores y proveedores de tecnologías en salud deberán transmitir al SIIFA la información de las respuestas a las devoluciones y glosas efectuadas por las entidades responsables de pago frente a las facturas electrónicas de venta del sector salud, priorizando la utilización de procesos informáticos de interoperabilidad entre estos y el SIIFA de acuerdo con lo establecido en el respectivo manual.
- Resolución 1912 (18 de septiembre). Hospital Universitario San Juan de Dios y Materno Infantil. Establece que el Ministerio de Salud y Protección Social apoyará la gestión y los trámites necesarios para la organización y puesta en funcionamiento del Hospital Universitario San Juan de Dios y Materno Infantil, en los aspectos que se demande o que haya a lugar en el marco de sus competencias para su entrada en operación por un periodo de seis meses. Dicho acompañamiento se realizará en los espacios dispuestos por el ministerio con las herramientas y medios necesarios para tal fin, sin que ello implique o se entienda que aquel personal prestará servicios al Hospital Universitario San Juan de Dios y Materno Infantil.
- Resolución 1888 (15 de septiembre). Resumen Digital de Atención en Salud en la Interoperabilidad de la Historia Clínica Electrónica (IHCE). Tiene por objeto adoptar el Resumen Digital de Atención en Salud (RDA) en el marco de la Interoperabilidad de la Historia Clínica Electrónica (IHCE) y establecer el mecanismo para la implementación en el ámbito nacional, de conformidad con lo establecido en la Ley 2015 del 2020 y en la Resolución 866 del 2021. El RDA estará conformado por los elementos de datos clínicos relevantes definidos en la Resolución 866 del 2021, o en la norma que la modifique o sustituya, los cuales constituyen la información mínima estandarizada para garantizar la interoperabilidad de la historia clínica electrónica y la continuidad del cuidado. El Ministerio de Salud y Protección Social dispondrá los componentes necesarios para realizar el intercambio de datos clínicos, los cuales se describen en el Anexo Técnico 1 “Lineamiento para la implementación del Resumen Digital de Atención en Salud-RDA, en el marco de la Interoperabilidad de la Historia Clínica Electrónica IHCE” que hace parte de la presente resolución.
- Resolución 1788 (4 de septiembre). Lineamientos técnicos y operativos para el fortalecimiento de la rehabilitación en salud. Con la presente resolución se adoptan los lineamientos técnicos y operativos para el fortalecimiento de la rehabilitación en salud en el marco del derecho fundamental a la salud, contenidos en el anexo técnico que será objeto de publicación en la página web del Ministerio de Salud y Protección Social, de conformidad con la parte considerativa del presente acto administrativo. La rehabilitación en salud está dirigida a todas las personas que presentan condiciones de salud que pueden generar necesidades de rehabilitación en salud relacionadas con diversos estados de alteración del funcionamiento humano de tipo transitorio o permanente, y que al ser transitorias pueden generar beneficios. Estas condiciones de salud se refieren a enfermedades (agudas o crónicas), trastornos, lesiones o traumatismos, u otras circunstancias como el embarazo, el envejecimiento, el estrés, una anomalía congénita o predisposición genética, entre otras.
- Circular 30 (4 de septiembre). Lineamientos entrada o salida de gametos masculinos o femeninos, preembriones o embriones del territorio nacional. Con la presente circular se imparten instrucciones para la entrada o salida de gametos masculinos o femeninos, preembriones o embriones del territorio nacional para la realización de procedimientos de reproducción humana asistida, así: la entrada o salida del territorio nacional de gametos masculinos o femeninos, preembriones o embriones solo podrá ser adelantada por IPS que realicen procedimientos de reproducción humana asistida debidamente habilitadas; las IPS que realicen procedimientos de reproducción humana asistida deberán verificar que se cuente con el consentimiento informado de los donantes, que se cumpla con los requisitos y condiciones tanto para la selección de los donantes como para el transporte de los gametos masculinos o femeninos, preembriones o embriones y que no exista violación al artículo 134 del Código Penal o la norma que lo modifique, adicione o sustituya. Es decir que no se trate de casos de tráfico de gametos, cigotos o embriones humanos; las IPS deberán reportar ante el Invima, dentro de las veinticuatro horas siguientes a la entrada o salida de gametos masculinos o femeninos, preembriones o embriones del territorio nacional, la información detallada en la presente circular, entre otras instrucciones.
- Resolución 1657 (14 de agosto). Modifica el periodo de transición para la implementación CIE-11. Mediante la presente resolución se modifican los artículos 3 y 4 de la Resolución 1442 del 2024, con el propósito de cambiar el periodo de transición para implementar la Clasificación Estadística Internacional de Enfermedades y Problemas de Salud Conexos (CIE-11). Por tanto, las entidades, organizaciones y actores tendrán un plazo máximo de hasta 36 meses contados desde la publicación para implementar la CIE-11. Durante dicho periodo deberán dar cumplimiento a las actividades necesarias previstas en el “Anexo 1” de la presente resolución y todas las demás disposiciones que el Ministerio de Salud y Protección Social emita para la adopción y la transición de la clasificación. La derogatoria de la Resolución 1895 del 2001 ocurrirá una vez finalice el periodo de los 36 meses de transición establecidos en la presente resolución.
- Resolución 1633 (11 de agosto). Marco técnico de infraestructura y equipamiento de edificaciones destinadas a la prestación de servicios de salud. Define el marco técnico normativo para la infraestructura y el equipamiento de edificaciones destinadas a la prestación de servicios de salud, estableciendo criterios técnicos para: (1) el diseño y el dimensionamiento de la infraestructura física, (2) el equipamiento adecuado de dichas edificaciones y (3) la adaptación al cambio climático, mediante la incorporación de medidas que fortalezcan la resiliencia de las construcciones destinadas a la prestación de servicios de salud.
- Ley 2006 (28 de julio). Fomenta la investigación científica y tecnológica para combatir microorganismos multirresistentes y prevenir la resistencia antimicrobiana. Tiene como objeto incentivar el estudio y la investigación intersectorial de los microorganismos multirresistentes y la resistencia antimicrobiana, así como disminuir su impacto en la salud pública mediante el desarrollo de sistemas de vigilancia y monitoreo. Con ello, busca fortalecer las estrategias de contención de la resistencia a los antimicrobianos de eficacia probada y promover el desarrollo de las capacidades informáticas y tecnológicas innovadoras necesarias para combatir esta problemática.
- Resolución 1444 (27 de junio). Política Pública del Talento Humano en Salud. Adopta la Política Pública del Talento Humano en Salud 2025-2035, la cual hace parte integral del presente acto administrativo, junto con su Documento Marco Orientador, de conformidad con la parte considerativa del presente acto. La Política Pública del Talento Humano en Salud 2025-2035 está dirigida a los trabajadores de la salud, y su objetivo general es fortalecer la gobernabilidad y la gobernanza del talento humano en salud mediante estrategias de planificación y gestión para la mejora de la disponibilidad, la distribución equitativa y la formación integral acorde con el análisis de la situación de salud de la población, que permitan el desempeño laboral en condiciones de empleo y trabajo digno y decente para la garantía del derecho fundamental a la salud.
- Ley 2466 (25 de junio). Modifica parcialmente normas laborales y se adopta una Reforma Laboral para el trabajo decente y digno en Colombia. Tiene por objeto adoptar una reforma laboral mediante la modificación del Código Sustantivo del Trabajo, la Ley 50 de 1990, la Ley 789 del 2002 y otras normas laborales; además se dictan disposiciones para el trabajo digno y decente en Colombia, buscando el respeto a la remuneración justa, el bienestar integral, la promoción del diálogo social, las garantías para el acceso a la seguridad social y la sostenibilidad de los empleos desde el respeto pleno a los derechos de los trabajadores, así como el favorecimiento a la creación de empleo formal en Colombia.
- Circular 020 (6 de junio). Aportes al Sistema de Protección Social Integral para la Vejez. Emite instrucciones para el reporte de información en el Registro Único de Afiliados (RUAF) y para el recaudo de aportes al Sistema de Protección Social Integral para la Vejez, Invalidez y Muerte de origen común a través de la planilla integrada de liquidación de aportes (PILA), en cumplimiento de la Ley 2381 del 2024 (Reforma Pensional). Por tanto, con el fin de identificar en el RUAF a las personas a las que no les aplica la transición prevista en el artículo 75 de la Ley 2381 del 2024, las Administradoras del Componente Complementario de Ahorro Individual (ACCAI) deberán reportar las personas vinculadas a este componente bajo los siguientes códigos: 230205 Protección, 230305 Porvenir, 230905 Skandia, 231005 Colfondos y 142305 Positiva Compañía de Seguros.
- Circular 022 (6 de junio). Instrucciones para el reporte de información casos incidentes de cáncer en Colombia. El Ministerio de Salud y Protección Social, de manera conjunta con el Instituto Nacional de Cancerología y la Superintendencia Nacional de Salud, expidieron la Circular 00000010 del 2 de julio del 2024 en la cual se implementó un plan de choque dirigido a concretar las acciones que garanticen la atención integral del cáncer a través de cinco componentes dirigidos a: (1) la organización de la red de servicios en salud; (2) el fortalecimiento de las competencias del talento humano en salud; (3) el programa de aseguramiento de la calidad; (4) la información, la educación y la comunicación, y (5) el seguimiento y el monitoreo. En razón del componente encaminado al seguimiento y el monitoreo en el marco del plan de choque previsto en la referida normativa, mediante la presente circular se solicita información específica para identificar las atenciones en salud con respecto a los casos incidentes de todos los tipos de cáncer en el país durante la etapa de diagnóstico, estadificación y tratamiento, con el propósito de orientar las decisiones en materia de política pública en salud dirigidas a la promoción de la salud y la prevención de la enfermedad.
- Circular 025 (10 de junio). Medidas para la prevención y el control de la fiebre amarilla, el dengue y otras arbovirosis. El Ministerio de Salud y Protección Social adopta medidas para la prevención y el control de la fiebre amarilla, dengue y otras arbovirosis durante ferias, fiestas y eventos con aglomeración de público focalizada y afluencia simultánea multiespacial. En dicho marco, se destacan las obligaciones para las IPS, así: implementar el monitoreo continuo de la notificación diaria de casos al SIGILA durante el evento y hasta dos semanas después; revisar y actualizar su Plan de Emergencia Hospitalaria; garantizar que el 100 % del personal de salud que prestará atención durante el evento esté capacitado en el manejo clínico de casos probables o confirmados; garantizar la disponibilidad de pruebas diagnósticas para la evaluación de la función hepática, incluyendo Aspartato Aminotransferasa (AST), Alanina Aminotransferasa (ALT) y bilirrubinas, como parte del manejo clínico de casos probables de fiebre amarilla durante el evento, entre otras medidas.
- Resolución 838 (7 de mayo). Comité Institucional para la articulación, la coordinación, el seguimiento y el cumplimiento de la Sentencia T-760 del 2008. Crea el Comité Institucional para la articulación, la coordinación, el seguimiento y el cumplimiento de la Sentencia T-760 del 2008 proferida por la Corte Constitucional, como instancia articuladora de las acciones y medidas que apunten al cumplimiento de los distintos mandatos proferidos en el marco de dicha sentencia. El comité estará integrado por los siguientes funcionarios: (1) el/la viceministro/a de Protección Social, quien lo presidirá; (2) el/la viceministro/a de Salud Pública y Prestación de Servicios; (3) el/la jefe de la Oficina de Calidad; (4) el/la director/a de Regulación de Beneficios, Costos y Tarifas del Aseguramiento en Salud; (5) el/la subdirector/a de Asuntos Normativos. El Comité Institucional podrá invitar a los servidores públicos y personal del Ministerio de Salud y Protección Social que considere necesarios, atendiendo los asuntos a tratar en la respectiva sesión.
- Circular 16 (30 de abril). Directrices ante la alerta regional de sarampión y riesgo de casos importados de interés en salud pública, sarampión y rubéola. En dicho marco, le corresponde a las IPS tanto públicas como privadas hacer énfasis en las siguientes actividades: vacunar a la población objetivo del Programa Ampliado de Inmunizaciones (PAI) con el esquema autorizado para el país y asegurar esquemas completos de vacunación hasta los 10 años, 11 meses y 29 días con Triple Viral. Además, asegurar la segunda dosis de triple viral a niños de 2, 3, 4, 5 años y cumplir con el reporte de la población vacunada al PAI Nacional según lineamientos nacionales, en cumplimento de las obligaciones con la Dirección Territorial de Salud (DTS) y Entidades Administradoras de Planes de Beneficios de Salud (EAPB); garantizar y verificar que el personal del área de la salud u otro personal que labora al interior de la institución y que estén en contacto con pacientes cuenten con el antecedente de vacunación de SR o SRP. Si no lo tienen o no recuerdan haber sido vacunadas con anterioridad, deben recibir una dosis de vacuna bivalente (SR), confirmar que el antecedente se encuentre registrado en el PAIWEB y en la hoja de vida de cada funcionario de la institución prestadora de salud. La vacuna de SR es gratuita, entre otras medidas.
- Resolución 1843 (29 de abril). Regula la práctica de evaluaciones médicas ocupacionales. Mediante la presente resolución el Ministerio del Trabajo regula la práctica de evaluaciones médicas ocupacionales, así como el manejo y el contenido de las historias clínicas ocupacionales, con alcance a todos los trabajadores del país, independientemente del sector económico, tipo de vinculación laboral o afiliación al Sistema General de Riesgos Laborales. En dicho contexto, se establecen las responsabilidades de los Prestadores de Servicios de Medicina de Seguridad y Salud en el Trabajo, empleadores y contratantes, ARL y trabajadores. También establece las evaluaciones médicas mínimas que deben realizar el empleador público y privado o contratante en forma obligatoria y su periodicidad, información básica requerida y personal responsable, entre otros temas. Así mismo, se define un periodo de seis meses para implementar la presente resolución.
- Resolución 691 (16 de abril). Emergencia sanitaria por fiebre amarilla. Atendiendo a la necesidad de contener la circulación activa del virus de la fiebre amarilla en todo el país hasta que haya transcurrido al menos ocho semanas epidemiológicas sin casos humanos ni epizootias y el deber Estatal de garantizar el derecho a la salud de toda la población en el territorio Colombiano, mediante la presente resolución se declarará la emergencia sanitaria en todo el territorio nacional y se tomarán medidas sanitarias, establecidas en la presente resolución, las cuales complementan y modifican lo dispuesto en las circulares externas 012 y 014 del 2025, expedidas por el Ministerio de Salud y Protección Social, cuyo objetivo es prevenir y controlar la propagación de la fiebre amarilla en el territorio nacional y mitigar sus efectos sobre la vida de las personas.
- Circular 012 (3 de abril). Preparación, organización y respuesta ante la situación de alerta y emergencia nacional por fiebre amarilla. Atendiendo a la Emergencia en Salud Pública por el brote de fiebre amarilla (FA) en el ámbito nacional en el 2024 y en lo corrido del 2025, el Ministerio de Salud y Protección Social emite instrucciones para la preparación, la organización y la respuesta ante la situación, así se actualiza la Circular 018 del 2017 en relación con la exigencia de certificación internacional o carné nacional de vacunación y deroga las circulares 018 del 2024 y 005 del 2025. En dicho marco le corresponde a las IPS públicas y privadas lo siguiente: dar cumplimiento a lo dispuesto en el protocolo de vigilancia en salud pública; analizar de forma periódica los indicadores de vigilancia del FA, confirmación y hospitalización por este evento en los COVE institucionales; garantizar la toma y el envío oportuno de tomas de muestra y tejidos para el envío al laboratorio departamental.
- Circular 011 (28 de marzo de diciembre). Instrucciones para la intensificación y el fortalecimiento de las acciones de vacunación, vigilancia y laboratorio por infección de tos ferina. Mediante la presente circular se imparten recomendaciones para el fortalecimiento de la vacunación y la vigilancia de la tos ferina para las EPS e IPS. Se precisa que el esquema de vacunación contra la tos ferina en Colombia (PAI) no incluye adolescentes ni adultos; no obstante, la vacunación en esta población cuenta como una estrategia complementaria particular para reducir la transmisión y proteger a la población vulnerable.
- Circular 010 (12 de marzo). Modificación de la entrada en vigor de la Circular 006 del 2025- Monitoreo antirretrovirales VIH. Modifica el plazo para la implementación de la Circular 006 del 2025, por tanto, la prescripción de los medicamentos financiados con la UPC que correspondan a las Denominaciones Comunes Internacionales (DCI) listadas en dicha circular, indicados en el tratamiento del VIH, se realizará de manera voluntaria a través de MIPRES desde el 24 de febrero y hasta el 31 de marzo del 2025 y a partir del 1.º de abril del 2025 será obligatoria de conformidad con las directrices establecidas en la citada circular.
- Resolución 0485 (27 de marzo). Expedición de los conceptos técnicos de viabilidad de los proyectos de inversión. La presente resolución tiene por objeto establecer los requisitos para la expedición de los conceptos técnicos de viabilidad de los proyectos de inversión cuya fuente de financiación o cofinanciación sea el Presupuesto General de la Nación-Ministerio de Salud y Protección Social o recursos de las Entidades Territoriales, y los proyectos de infraestructura física, equipamiento fijo y dotación biomédica, considerados de control especial de oferta para la prestación de servicios de salud cuyo fin último es el fortalecimiento de la capacidad instalada para la prestación del servicio de salud.
- Resolución 465 (25 de marzo). Modifica Resolución 3100-Habilitación IPS. Modifica algunos aspectos de la Resolución 3100 del 2019, en relación con el estándar de infraestructura, así: (1) modificar las condiciones de los consultorios donde se atiendan menores de 5 años, eliminado la barrera física fija o móvil entre las áreas de entrevista y exámenes; (2) establecer el uso obligatorio de los emblemas estrella de la vida y el emblema protector de la Misión Médica, y (3) no requerir el ambiente de simulación de tratamiento en el servicio de radioterapia cuando la tecnología incorpore la simulación del tratamiento.
Así mismo, en el estándar de Talento Humano se precisa lo siguiente: (1) el procedimiento de vacunación se puede realizar en los servicios de salud cuyo talento humano haya adquirido las competencias para administrar inmunobiológicos; (2) la constancia de asistencia de las acciones de formación continua en gestión operativa de la donación exigido para el coordinador operativo de trasplantes será expedida por el Instituto Nacional de Salud (INS); (3) el INS será la entidad responsable de emitir los lineamientos para la expedición de la constancia de asistencia de las acciones de formación continua en detección y cuidado del donante, y (4) en el servicio de transporte asistencial en ambulancia aérea el talento humano deberá ser técnico profesional o tecnólogo en atención prehospitalaria.
En cuanto al estándar de Procesos Prioritarios se determina que los prestadores que instalen cámaras de videovigilancia al interior de las áreas o ambientes donde se presten servicios de salud para grabar la realización de procedimientos en salud, deben contar con un documento escrito en el que se evidencie la autorización de la grabación, el cual deberá ser firmado por los pacientes o sus representantes y por el talento humano en salud responsable del procedimiento; este documento hará parte de la historia clínica, en cumplimiento de la Sentencia T-144 del 2024.
- Resolución 0435 (14 de marzo). Reglamenta el reporte de los hechos vitales y se adopta la aplicación tecnológica Registro Único de los Afiliados-Nacimientos y Defunciones (RUAF ND). Todos los nacimientos y defunciones ocurridos en el territorio nacional deberán ser reportados al Ministerio de Salud y Protección Social mediante la aplicación tecnológica Registro Único de los Afiliados-Nacimientos y Defunciones (RUAF ND).
Los hechos vitales que no sean atendidos por el sector salud y de los cuales se tenga conocimiento deberán ser notificados a la Secretaría de Salud de la jurisdicción correspondiente, para que esta los reporte al Ministerio de Salud y Protección Social.
Corresponde al Instituto Nacional de Medicina Legal y Ciencias Forenses, en el marco de sus competencias, asegurar que las defunciones correspondientes a necropsias médico-legales sean reportadas al Ministerio de Salud y Protección Social mediante la aplicación tecnológica RUAF ND, incluidas aquellas realizadas por la Unidad de Búsqueda de Personas Desaparecidas.
- Circular 08 (10 de marzo). Instrucciones para la Resolución 214 del 2022-Requisitos sanitarios que deben cumplir los dispositivos médicos sobre medida bucal (DMSMB). Determina que no debe existir ningún tipo de publicidad dirigida al público general o a los pacientes con respecto a los dispositivos médicos sobre medida bucal o los servicios prestados por estos establecimientos comerciales, con el fin de evitar que se induzca a los consumidores a adquirir productos sin una adecuada orientación profesional. Así mismo, el odontólogo es el único facultado para prescribir el dispositivo médico sobre medida bucal, mientras que la responsabilidad del control de calidad en cuanto a su fabricación y reparación recae exclusivamente en el director técnico o en la persona delegada por este, excluyendo a quienes participen directamente en dichos procesos.
El director técnico de un establecimiento que fabrique o repare DMSMB debe poseer una certificación o diploma de tecnólogo en mecánica dental, o de técnico profesional en mecánica dental, o de técnico laboral en mecánica dental, expedida por instituciones educativas de Trabajo y Desarrollo Humano, o universidades con estos programas.
- Circular 06 (24 de febrero). Instrucciones para el reporte de prescripción y monitoreo en MIPRES de antirretrovirales para el VIH. Con la presente circular se imparten instrucciones para monitorear y evaluar el acceso a las tecnologías en salud en la prestación de los servicios en salud, por lo cual se permite la prescripción, el direccionamiento, el suministro y el reporte de los medicamentos descritos en la presente circular, incluyendo los medicamentos en combinaciones a dosis fijas a través de MIPRES, los cuales se identifican en su denominación común internacional (DCI) acorde con la Resolución 3311 del 2018 o la norma que la modifique, sustituya o derogue. De esta manera, corresponde a los prestadores de servicios de salud realizar el registro de las prescripciones de los medicamentos financiados con la UPC que contengan las DCI enlistadas en esta circular.
- Resolución 050 (16 de enero). Vigencia de la habilitación de las Redes Integrales de Prestadores de Servicios de Salud (RIPSS). Cambia el artículo 10 de la Resolución 1441 del 2016 modificado por las resoluciones 087 y 1367 del 2024; por tanto, la habilitación de las RIPSS tendrá una vigencia de cinco años, a partir de su habilitación a través del módulo de redes, sin perjuicio de que la Superintendencia Nacional de Salud, en ejercicio de sus funciones de seguimiento al cumplimiento de los estándares y criterios de permanencia de Red y de inspección, vigilancia y control, adopte las medidas pertinentes sobre la habilitación. La vigencia de la habilitación de las RIPSS que se venza a partir del 31 de enero del 2025 se ampliará por un año o hasta la entrada en funcionamiento anticipada de las Redes Integrales e Integradas Territoriales de Salud.
- Resolución 191 (5 de febrero). Resultados de la convocatoria para la selección de colegios profesionales del área de la salud en los que se delegarían funciones públicas. Con base en el procedimiento estipulado en la Resolución 2235 del 2024 la Dirección de Desarrollo de Talento Humano en Salud del Ministerio de Salud y Protección Social evaluó las postulaciones presentadas por los colegios profesionales de la salud, verificando el cumplimiento de los requisitos documentales y los criterios de evaluación establecidos. Por tanto, se identificó que los siguientes colegios profesionales de la salud cumplen con los requisitos: Organización Colegial de Enfermería (OCE), Colegio Colombiano de Fisioterapeutas (COLFI), Colegio Colombiano de Odontólogos (CCO), Colegio Colombiano de Fonoaudiólogos (CCF), Colegio Médico Colombiano, Colegio Colombiano de Terapia Ocupacional (CCTO), Colegio Colombiano de Nutricionistas Dietistas (COLNUD), Colegio Federación Colombiana de Optómetras (FEDOPTO), Colegio Colombiano de Instrumentación Quirúrgica, Colegio Colombiano de Terapeutas Respiratorios (CCTR) y Colegio Nacional de Químicos Farmacéuticos de Colombia.
- Circular 02 (27 de enero). Preparación, organización y respuesta ante el brote de fiebre amarilla en el Tolima. A través de la presente circular se imparten instrucciones complementarias y transitorias a la Circular 018 del 2024, hasta que se establezca el control de la emergencia sanitaria por brote de fiebre amarilla en el departamento del Tolima y se superen las siguientes condiciones señaladas en la Circular 018 del 2024: municipio o departamento en los últimos seis meses con ausencia de casos tanto en humanos como epizootias; vigilancia en salud pública sensible y funcionando en los ámbitos institucional y comunario; vigilancia de epizootias operando; coberturas de vacunación para FA≥80 % en el corredor endémico mediante barrido documentado donde se confirmó la presencia del caso en población de 1 a 59 años en el corredor endémico.
En dicho contexto las IPS con servicios de urgencias activos deberán reportar con carácter obligatorio y a diario las capacidades hospitalarias para emergencias en el siguiente enlace: https://ee.humanitarianresponse.info/x/KMLBnHKT y sus afectaciones en el siguiente vínculo: https://forms.office.com/r/RfUrhafdwb?oriqin=IprLink. El reporte se hará a las 18:00 horas.
- Circular 01 (3 de enero). Solicitud de información de acciones de tutela interpuestas para la protección del derecho fundamental a la salud. Mediante la Sentencia T-760 del 2008 la Corte Constitucional impartió una serie de directrices tendientes a superar las fallas evidenciadas en el SGSSS, de las que hace parte el mandato trigésimo, que ordenó al Ministerio de Salud y Protección Social, entre otros, presentar a la citada Corporación un reporte anual de medición de las acciones de tutela incoadas para la protección del derecho a la salud.
Así, las EPS de los regímenes contributivo y subsidiado, las EPS Indígenas, las Entidades Adaptadas, las IPS, las Entidades Territoriales, el Instituto Nacional Penitenciario y Carcelario (Inpec) y los regímenes de excepción, deberán reportar al ministerio la información relacionada con las acciones de tutela interpuestas en su contra para la protección del derecho a la salud, en el anexo técnico que hace parte integral de esta circular y bajo las especificaciones allí previstas. El reporte se hará a través de la Plataforma de Intercambio de Información (PISIS_ del Sistema Integral de Información de la Protección Social (SISPRO).
E. Inspección, vigilancia y control
- Resolución 2025320030009640-6 (31 de septiembre). Modifica medidas Nueva EPS S. A. En el marco de la medida cautelar decretada a la Nueva EPS S. A. y con ocasión de las fallas estructurales que se relacionan con: (1) las dificultades en la estabilización del procesamiento y la auditoría de cuentas médicas; (2) la inconclusa formalización de acuerdos de voluntades con la red; (3) el retraso en la ejecución del plan estratégico de modernización tecnológica, y (4) las consecuentes dificultades en la disposición de la información a la contralora para el giro de los recursos en el marco de la medida cautelar de cesación, que sin el seguimiento permanente podrían afectar el flujo de recursos a la red prestadora y proveedora de servicios y tecnologías en salud, toda vez que las fallas aludidas dificultan el completo control previo de la postulación y el giro de recursos para la protección de la debida destinación de los recursos del SGSSS, se hacen modificaciones a la medida cautelar decretada.
Así se modifican los artículos primero y tercero de la Resolución 2025320030006237-6 del 31 de julio del 2025 frente al control pretendido para la postulación y el giro de recursos de esta EPS vigilada debido a que se requiere una transición prudente que garantice las condiciones mínimas que permitan realizar el control previo al giro de los recursos. Así mismo, lo ordenado a la ADRES comenzará a regir a partir de febrero del 2026, con el soporte del informe de viabilidad del giro emitido por la contralora para llevar a cabo la ejecución del giro de los recursos programados por la Nueva EPS.
- Resolución 2025920050007532-6 (4 de septiembre). Amplía el plazo para pagar la contribución a favor de la Supersalud. De este modo, todos los sujetos pasivos de la contribución de vigilancia a favor de la Superintendencia Nacional de Salud pagarán dicho tributo desde el 14 de julio del 2025 por cada tipo de vigilado hasta el 30 de septiembre del 2025. Los contribuyentes podrán realizar objeciones contra el recibo de pago hasta el 19 de septiembre del 2025; vencido este plazo no habrá lugar a tramitar objeciones y serán rechazadas de plano.
- Circular 2025151000000009-5 (11 de agosto). Reporte de información de los gestores farmacéuticos. A través de la presente circular se emiten instrucciones adicionales a la Circular 047 del 2007 a los gestores farmacéuticos para el reporte de información a la Superintendencia Nacional de Salud-Superintendencia Delegada para Operadores Logísticos de Tecnologías en Salud y Gestores Farmacéuticos, relacionada con acuerdos de voluntades con Entidades Responsables de Pago, establecimientos farmacéuticos (puntos de dispensación), dispensación de medicamentos y dispositivos médicos, así como tecnologías en salud con dificultades de dispensación para efectos de labores de inspección, vigilancia y control a estos.
- Resolución 2025320030006459-6 (6 de agosto). Modifica la Resolución 2025320030006237-6-Medidas Nueva EPS. Modifica los artículos 1 y 3 de la Resolución 2025320030006237-6 del 31 de julio del 2025, por la cual se ordenó la medida cautelar de cesación provisional de las acciones que ponen en riesgo la vida e integridad física de los pacientes y el destino de los recursos del Sistema de Salud a la Nueva EPS S. A. Así, se precisa que la fecha para la emisión del informe de auditoría por parte de la contralora, que incluya la recomendación del giro de los recursos del SGSSS, será a partir del 1.º de octubre del 2025. Por tanto, lo ordenado a la ADRES comenzará a regir a partir del 1.º de octubre del 2025, con el soporte del informe de auditoría emitido por la contralora designada, para llevar a cabo la ejecución del giro directo programado por la Nueva EPS S. A.
- Circular 2025151000000008-5 (1.º de agosto). Modifica instrucciones de la Circular Externa 006 del 2018 para el reporte de información relacionada con el flujo de recursos del SGSSS. La Superintendencia Nacional de Salud expide instrucciones de obligatorio cumplimiento para el reporte de información correspondiente al flujo de recursos que financian el SGSSS, con el fin de adelantar las acciones de inspección, vigilancia y control. En dicho marco, la ADRES deberá disponer la información que se detalla en la presente Circular Externa, por medio de acceso directo a su base de datos, garantizando la disponibilidad de la información histórica hasta el último periodo disponible reportado. El cargue de la información tiene una periodicidad mensual.
- Circular 2025151000000007-5 (30 de mayo). Instrucciones para adelantar y hacer seguimiento al proceso de conciliación, depuración y saneamiento de las cuentas por pagar entre EPS y las ABP. Actualiza la Circular 011 del 2020, con el fin de realizar el seguimiento al proceso de conciliación y el saneamiento de las cuentas por cobrar y por pagar entre las Entidades Responsables de Pago y las IPS y demás proveedores de servicios y tecnologías en salud. Las EPS de los regímenes contributivo y subsidiado, incluyendo las indígenas, las Entidades Adaptadas y las Entidades Territoriales del orden departamental y distrital deberán adelantar todas las gestiones administrativas tendientes a realizar el proceso de conciliación, depuración y saneamiento de las cuentas por pagar con los prestadores de servicios de salud, uniones temporales, gestores farmacéuticos y operadores logísticos de tecnologías en salud.
En dicho proceso no se deberán priorizar los acreedores que pertenezcan al mismo grupo empresarial de la EPS o aquellos con los que las cuentas por pagar no superen sesenta días de mora o aquellos con los que no registre glosas. La entidad deberá informar a su acreedor que tiene la intención de incluirlo en el cronograma para su participación, con el objetivo de acordar una fecha para el inicio de la mesa de conciliación.
- Resolución 2025320030006237-6 (31 de julio). Medida cautelar a Nueva Empresa Promotora de Salud S. A. La Superintendencia Nacional de Salud ordena con carácter inmediato a la Nueva EPS S. A., la medida cautelar de cesación provisional de las acciones que ponen en riesgo la vida e integridad de los afiliados y los recursos del SGSSS. Por lo anterior Nueva EPS deberá, entre otras medidas, poner a disposición del contralor designado en el marco como mínimo la siguiente información: (1) la política de pagos, metodología de pagos y acto administrativo de conformación del Comité de Pagos; (2) detalle de la aplicación de la metodología de pagos aplicada en el periodo correspondiente y acta de Comité de Pagos donde se llevó a cabo la aprobación de la postulación de recursos del SGSSS con sus respectivos soportes, entre otra información.
- Decreto 527 (14 de mayo). Autorización especial para las EPS del régimen contributivo con afiliados en el régimen subsidiado. Mediante el presente decreto se adiciona una autorización especial con reglas específicas que permita a las EPS del régimen contributivo, con afiliados en el régimen subsidiado, continuar garantizando la prestación de los servicios en salud a esta población. Para lo anterior, la Superintendencia Nacional de Salud actualizará de manera inmediata el certificado de autorización de funcionamiento del régimen contributivo para operar en el régimen subsidiado, a las EPS que a la expedición del presente decreto se encuentren autorizadas en el régimen contributivo y cuenten con afiliados del régimen subsidiado, incluidas aquellas que tengan medida de vigilancia especial o de intervención forzosa administrativa para administrar. El certificado de autorización de funcionamiento se expedirá en el ámbito territorial donde la EPS tiene población del régimen subsidiado. Las EPS con autorización especial, conforme a lo dispuesto en el presente artículo, no estarán obligadas a acreditar capital adicional. No obstante, estas EPS tendrán una limitación de la capacidad de afiliación para realizar nuevas afiliaciones para aceptar traslados en el régimen subsidiado y recibir afiliados del régimen subsidiado hasta que acrediten el cumplimiento del capital adicional.
- Circular 011 (8 de marzo). Instrucciones para la intensificación y el fortalecimiento de las acciones de vacunación, vigilancia y laboratorio por infección de tos ferina. Mediante la presente circular se imparten las siguientes recomendaciones para el fortalecimiento de la vacunación y la vigilancia de la tos ferina, para las EPS e IPS.
- Garantizar, conforme a los lineamientos del PAI, el inicio, la continuación y la finalización de los siguientes esquemas de vacunación: (1) población gestante: vacunación con Tdap a partir de la semana 26 de gestación, y en caso de lugar rural disperso desde la semana 20; (2) para los niños y niñas: la vacuna pentavalente se aplica a los 2, 4, 6 y 18 meses y DTP a los 5 años de vida.
- Cumplir el protocolo y las guías de práctica clínica de tos ferina y eliminar las barreras administrativas que dificulten el acceso oportuno, el diagnóstico y el tratamiento de los casos.
- Asegurar que su red prestadora de servicios garantice la toma de muestra, diagnóstico, tratamiento y manejo integral de los casos probables y confirmados de tos ferina.
- Garantizar la adherencia y la continuidad del tratamiento de los casos probables y confirmados de tos ferina.
- Establecer un diagnóstico diferencial una vez el caso probable de tos ferina ha sido descartado por el laboratorio.
Así mismo, el esquema de vacunación contra la tos ferina en Colombia (PAI) no incluye adolescentes ni adultos; no obstante, la vacunación en esta población cuenta como una estrategia complementaria particular para reducir la transmisión y proteger a la población vulnerable.
Resolución 2025300000000357-6 (28 de enero). Reporte de acreditación por parte de contralores que ejerzan el cargo en más de una medida de control. Adiciona y modifica el artículo 9 de la Resolución 2599 del 2016, por la cual se dictaron disposiciones relacionadas con inscripción, designación, fijación de honorarios, posesión, funciones, obligaciones, seguimiento, sanciones, reemplazo y otros asuntos de los agentes interventores, liquidadores y contralores de las entidades objeto de medidas especiales de toma de posesión e intervención forzosa administrativa prevista en el artículo 68 de la Ley 1753 del 2015, por parte de la Superintendencia Nacional de Salud. De esta manera, para el adecuado desempeño del cargo los interventores, liquidadores y contralores en relación con la exigencia de la capacidad técnica se pretende ajustar la forma como informarán a la Superintendencia lo relativo a la acreditación por parte de contralores que ejerzan el cargo en más de una medida de control, la fijación de honorarios de manera que los agentes puedan acreditar de manera clara y transparente los requisitos exigidos por el artículo 9 para esos efectos.
CONTÁCTENOS
Mayor Información Tel: (+57) 601 312 4411 –Fax: (+57) 601 312 1005 Cra 4 No. 73 – 15 Bogotá D.C.
COPYRIGHT © 2022 – Todos los derechos reservados
Prohibida su reproducción parcial o total sin autorización escrita de su titular
Powered by windowschannel.com